胰岛素如何调控奖赏系统和行为动机?
中脑边缘多巴胺通路是脑内奖赏系统最重要的组成部分之一。在过去的几十年中,该通路已经被证明在奖赏搜索、强化学习、行为动机和执行控制等方面起到关键作用。胰岛素作为调节饮食摄入的主要肽类,可以跨越血脑屏障,直接作用于中枢奖赏系统的中脑边缘多巴胺通路。
刘帅研究员及合作者之前的一系列研究阐明了胰岛素在奖赏系统及摄食行为中的作用机制 (Nature Neuroscience, 2013;Nutrition and Diabetes, 2013;PNAS, 2016)。在之后对人类的影像研究和数据建模分析中,科学家发现胰岛素确实可以通过作用于中脑边缘多巴胺系统,降低被试对美味食物的评分(Nature Communications, 2017),进一步确证了刘帅研究员及合作者之前研究的结论。然而,胰岛素在同是多巴胺奖赏通路中的腹侧被盖区和伏隔核的作用却是是截然相反的,这个问题始终困扰着领域内的科学家。
基于刘帅研究员及合作者在胰岛素中枢奖赏机制研究中的一系列贡献,Experimental Neurology (5 year IF: 4.682)杂志编辑邀请刘帅研究员及合作者为本期特刊“脑的胰岛素抵抗”撰写论文。该论文系统地比较了胰岛素分别在腹侧被盖区和伏隔核,在神经元层面(受体表达、兴奋性传递、多巴胺释放、多巴胺转运)和行为层面(摄食行为与药物相关行为)的作用效果。结论提示胰岛素在腹侧被盖区降低兴奋性传入并减少神经元周围多巴胺释放,而在伏隔核则借助胆碱能中间神经元增加兴奋性并增加末端的多巴胺释放。反映在行为学上,腹侧被盖区的胰岛素能有效降低食物线索的价值并降低奖赏性食物摄入,伏隔核的胰岛素能增强奖赏搜索行为和药物诱导的强迫行为。
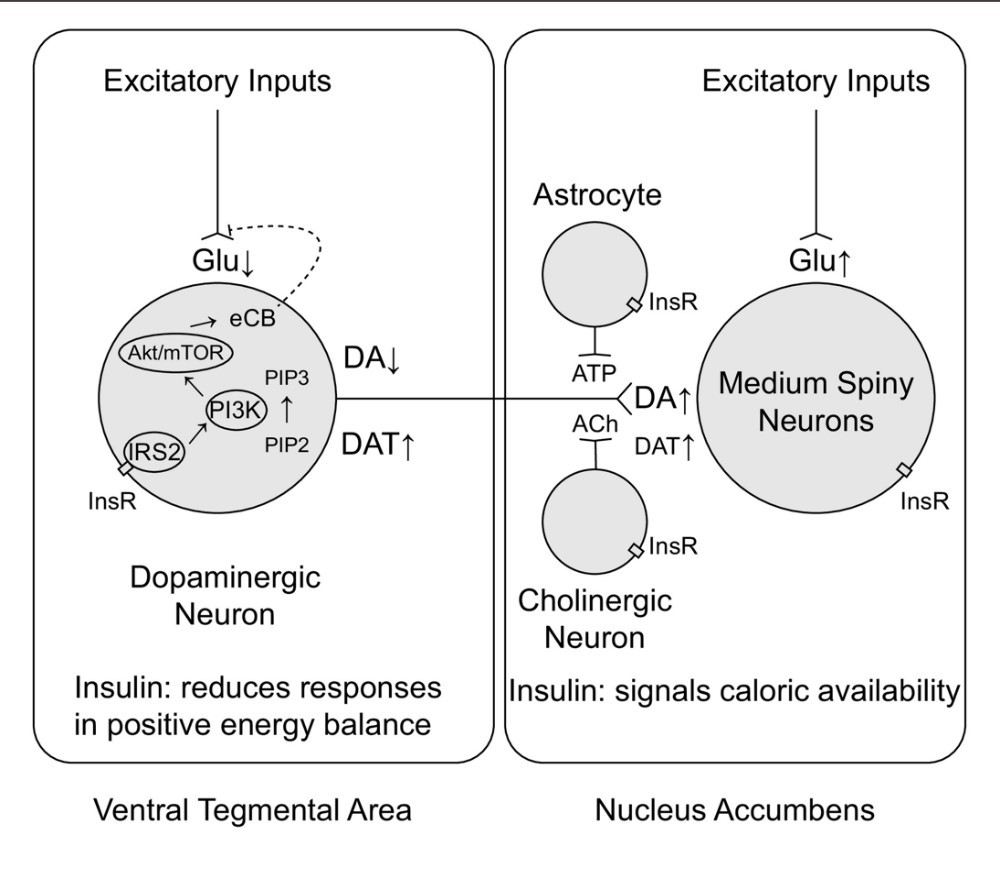
通过对大量文献的分析论证,刘帅研究员及合作者提出的观点是,胰岛素在奖赏系统的脑区特异性能够优化个体对外部环境和本身能量状态的应答。伏隔核的胰岛素能在进食前期,标识目前的能量增量并通过多巴胺释放强化对高能量食物的响应,而当个体处于饱食状态下,腹侧被盖区的胰岛素通过切换神经元放电模式降低食物价值,胰岛素在两者的作用时间维度和功能上均存在差异。这样,胰岛素在奖赏系统不同脑区的相反作用在本论文的理论框架下得到了和谐的统一。解码胰岛素在中脑边缘系统的精细调控作用,将在针对代谢疾病、药物滥用和摄食疾病更有效的治疗中起到至关重要的作用。
该研究得到了国家自然科学基金项目(31800856)、上海市科委浦江人才计划(18PJ1402600)、上海市卫计委项目(ZK2015B01,201540114)和加拿大健康研究院项目(FDN-147473)的资助。
参考文献:
1. S. Liu and S.L. Borgland, 2019. Insulin actions in the mesolimbic dopamine system, Experimental Neurology, https://doi.org/10.1016/j.expneurol.2019.113006
2. S. Liu, A.K. Globa, F. Mills, L. Naef, M. Qiao, S.X. Bamji, S.L. Borgland, 2016. Consumption of palatable food primes food approach behaviour by rapidly increasing synaptic density in the VTA. PNAS, 113(9): 2520-2525. DOI: 10.1073/pnas.1515724113
3. S. Liu*, G. Labouèbe*, S. Karunakaran, S.M. Clee, S.L. Borgland, 2013. Effect of insulin on excitatory synaptic transmission onto dopamine neurons of the ventral tegmental area in a mouse model of hyperinsulinemia. Nutrition & Diabetes. 16;3:e97.
4. G. Labouèbe*, S. Liu*, C. Dias, H. Zou, J.C. Wong, S. Karunakaran, S.M. Clee, A.G. Phillips, B. Boutrel, S.L. Borgland, 2013. Insulin induces long-term depression of ventral tegmental area dopamine neurons via endocannabinoids. Nature Neuroscience. 16(3):300-8.
5. L.J. Tiedemann, S.M. Schmid, J. Hettel, K. Giesen, P. Francke, C. Büchel, S. Brassen, 2017. Central insulin modulates food valuation via mesolimbic pathways. Nature Communications. 8:16052. doi: 10.1038/ncomms16052.
